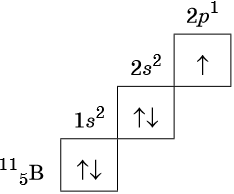
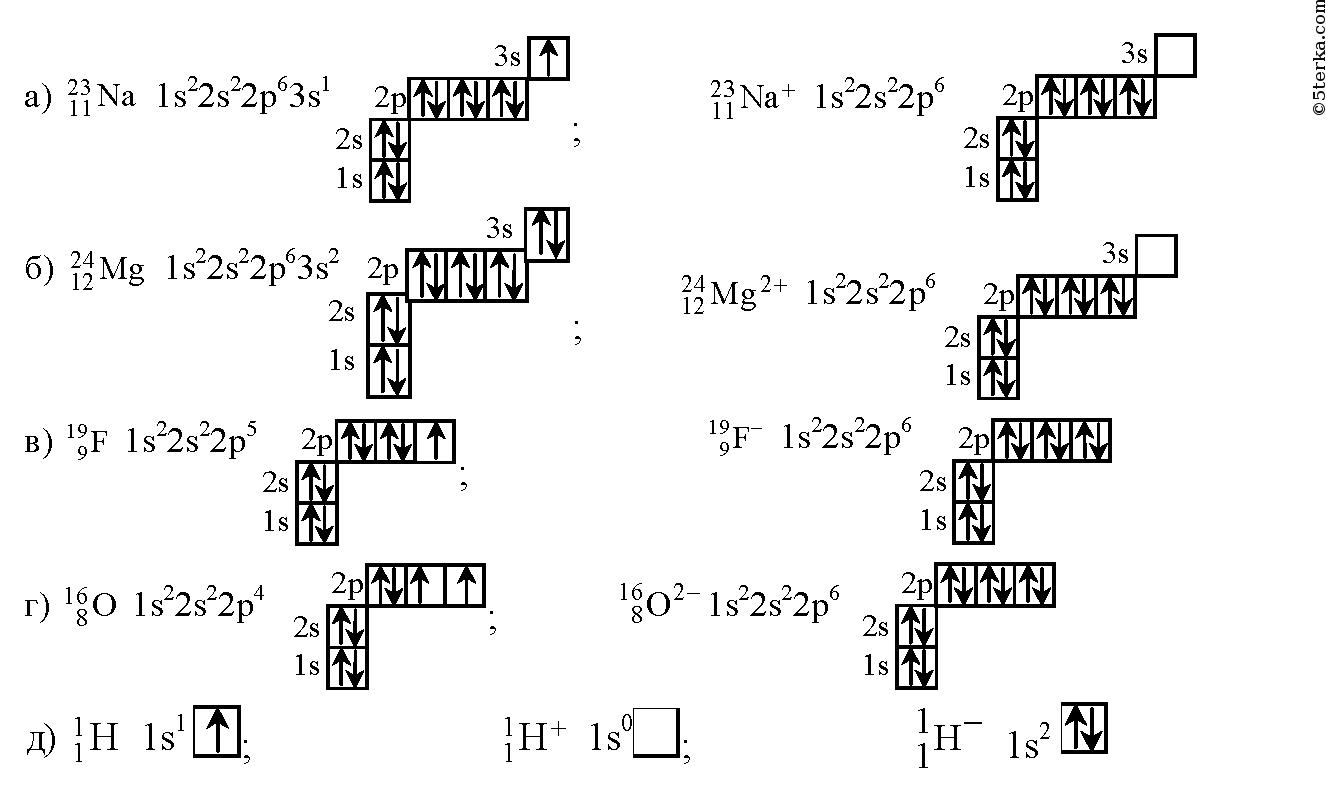
Электронная схема фтора
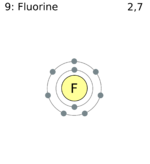
Исследована твердотельная фтор-ионная электрохимическая ячейка
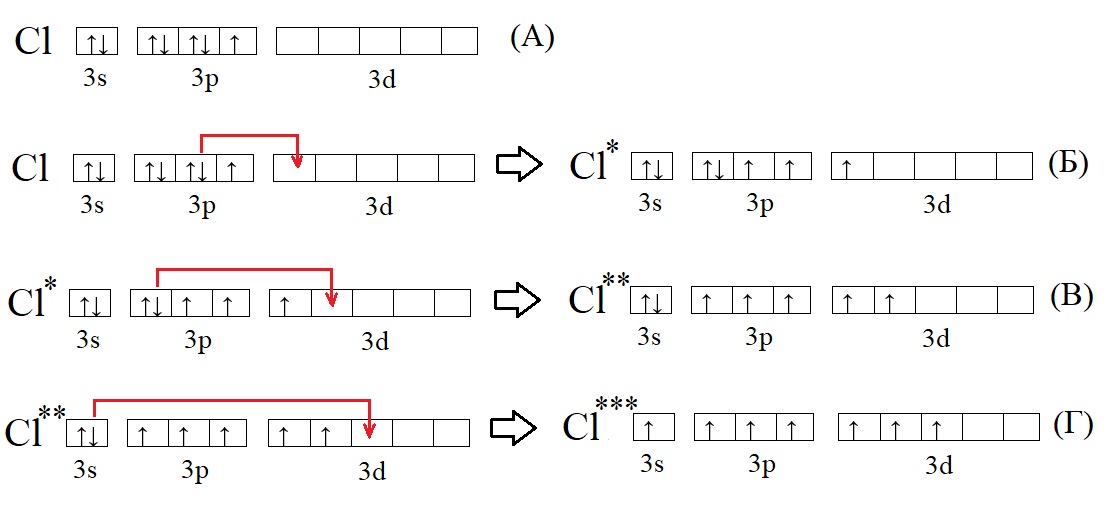
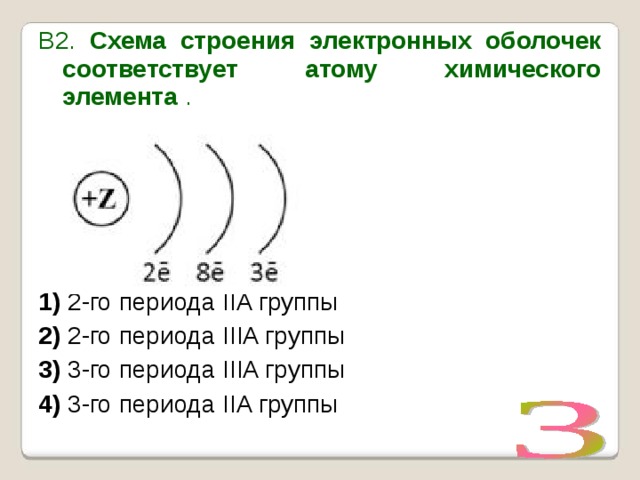
Определите, атомы каких из указанных в ряду элементов имеют в возбуждённом состоянии электронную конфигурацию внешнего энергетического уровня ns 1 np 3 nd 1. Запишите в поле ответа номера выбранных элементов. Электронная конфигурация ns 1 np 3 nd 1 в возбужденном состоянии показывает, что на внешнем слое у атома будет расположено 5 электронов, значит нужны элементы из пятой группы главной подгруппы, таких три: азот, фосфор и мышьяк. Однако атом азота не может переходить в возбужденное состояние, так как на втором энергетическом уровне нет d — подуровня, следовательно, ответ: фосфор и мышьяк.


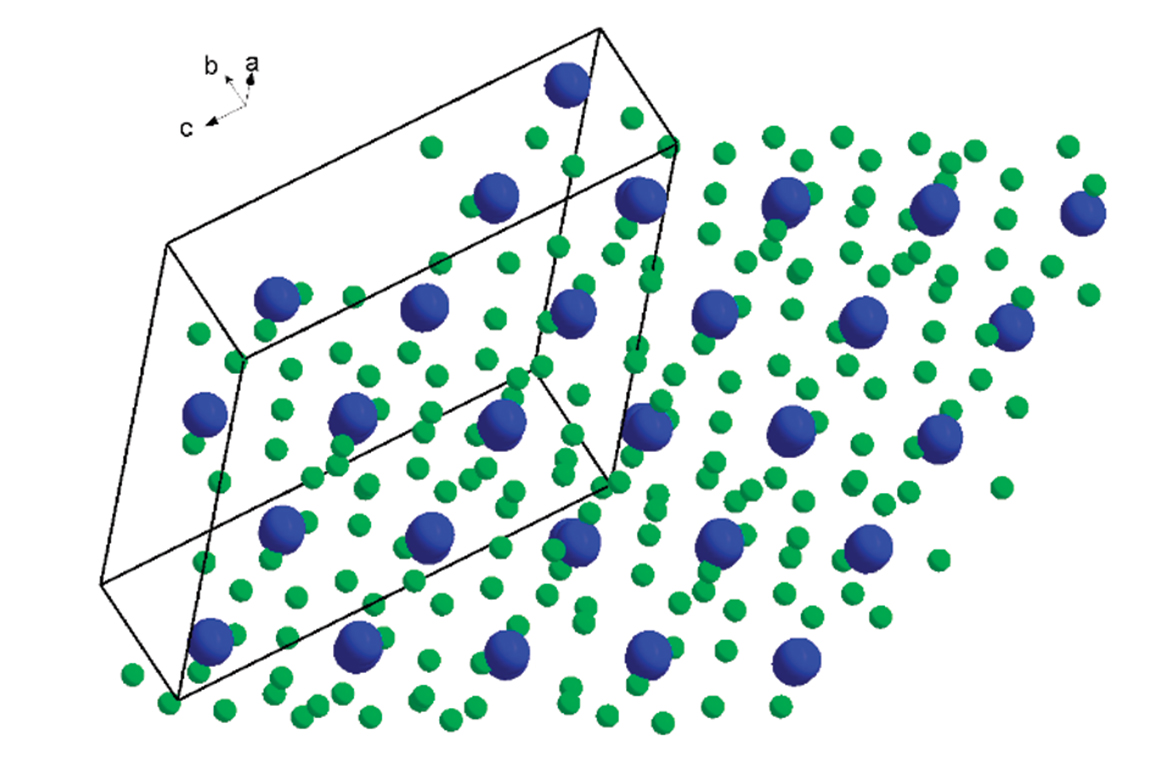





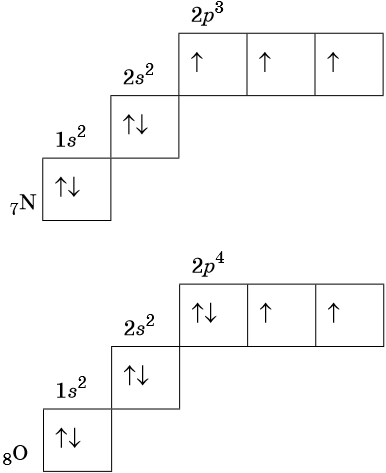

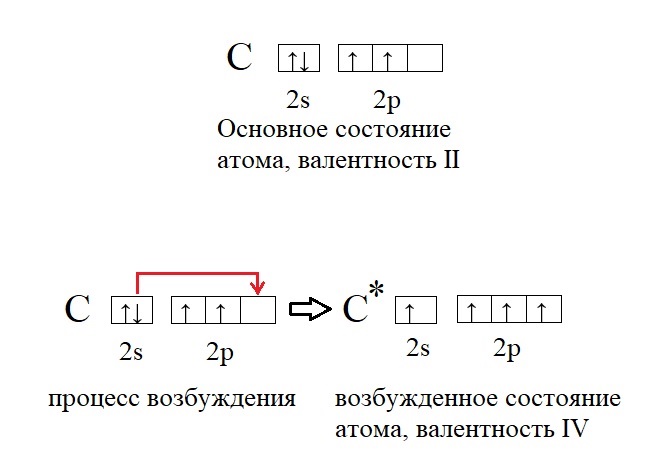
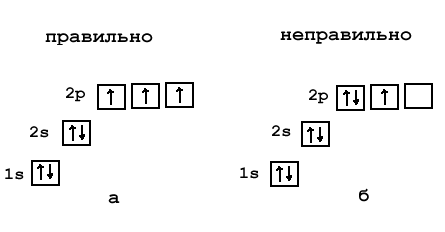
Фтор — элемент главной подгруппы седьмой группы, второго периода периодической системы химических элементов Менделеева, с атомным номером 9. Обозначается символом F Fluorum. Фтор — чрезвычайно химически активный неметалл и самый сильный окислитель, является самым лёгким элементом из группы галогенов.
- 6.6. Особенности электронного строения атомов хрома, меди и некоторых других элементов
- Рубрика: ЕГЭ - химия для чайников.
- Носителями зарядов в твердотельной FIB вместо ионов лития выступают ионы фтора.
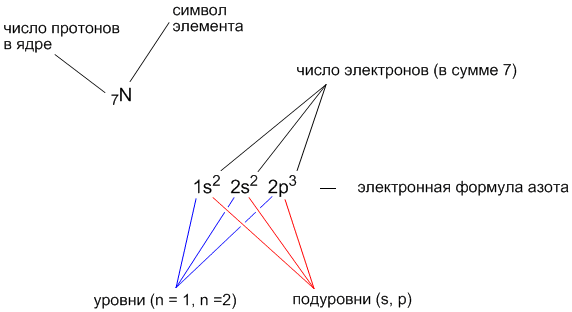
- На этой странице показаны электронные конфигурации нейтральных атомов в их основных состояниях. Для каждого атома подоболочки даны сначала в краткой форме, затем со всеми выписанными подоболочками, за которыми следует число электронов на оболочку.


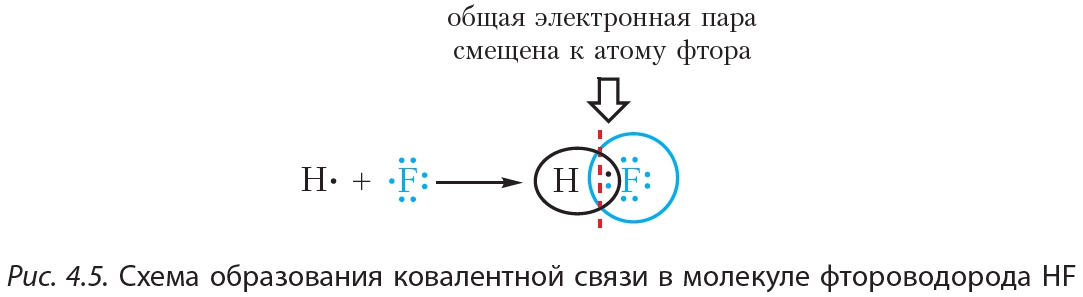
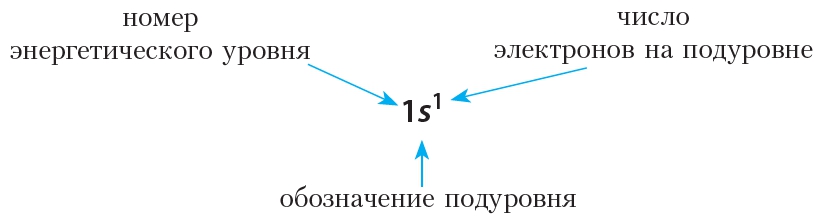


Фтор имеет 9 электронов, заполним электронные оболочки в описанном выше порядке:. Атомы фтора в соединениях имеют степени окисления 0, Степень окисления - это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная электроны несут отрицательный заряд , если заряд уменьшается, то степень окисления положительная. Валентность фтора характеризует способность атома F к образованию химических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами.