Как связана энтальпия с внутренней энергией

Вы точно человек?
Поскольку химическое превращение обычно сопровождается высвобождением или поглощением определенного количества теплоты, оно, как и другие явления природы в том числе электрические и магнитные , сопровождающиеся тепловыми эффектами, подчиняется фундаментальным принципам началам термодинамики. Химическая термодинамика определяет, в первую очередь, условия такие, как температура и давление протекания химических реакций и равновесных состояний, которых они достигают. Анализ тепловых явлений базируется на трех фундаментальных принципах, подтвержденных данными многочисленных наблюдений.








Внутренняя энергия. Превращения энергии при химических реакциях. Энергетические эффекты при фазовых переходах. Термохимические расчеты.
- В молекулярно-кинетической теории внутренняя энергия составляется из кинетической энергии всех частиц, потенциальной энергии взаимодействия молекул и энергии колебательного движения атомов т.
- Забыли пароль?
- Энтальпия системы от греч. Энтальпия имеет размерность энергии кДж.
- Таким образом, изменение внутренней энергии идеального газа равно произведению средней теплоемкости при постоянном объеме на разность температур газа. Э н т а л ь п и я теплосодержание насыщенного газа — количество теплоты, необходимое для повышения температуры 1 кг вещества от аб солютного нуля до пара заданной температуры.
- Основы химической термодинамики.
- Энтальпия от греч. При постоянной р изменение энтальпии равно количеству теплоты, подведённой к системе, поэтому энтальпия называется часто тепловой функцией или теплосодержанием.
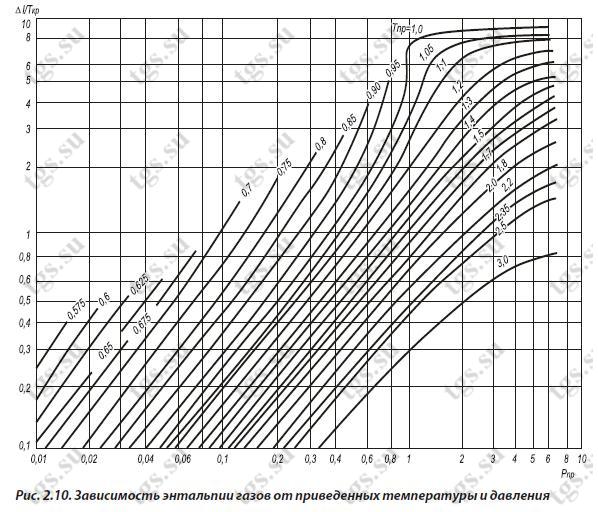


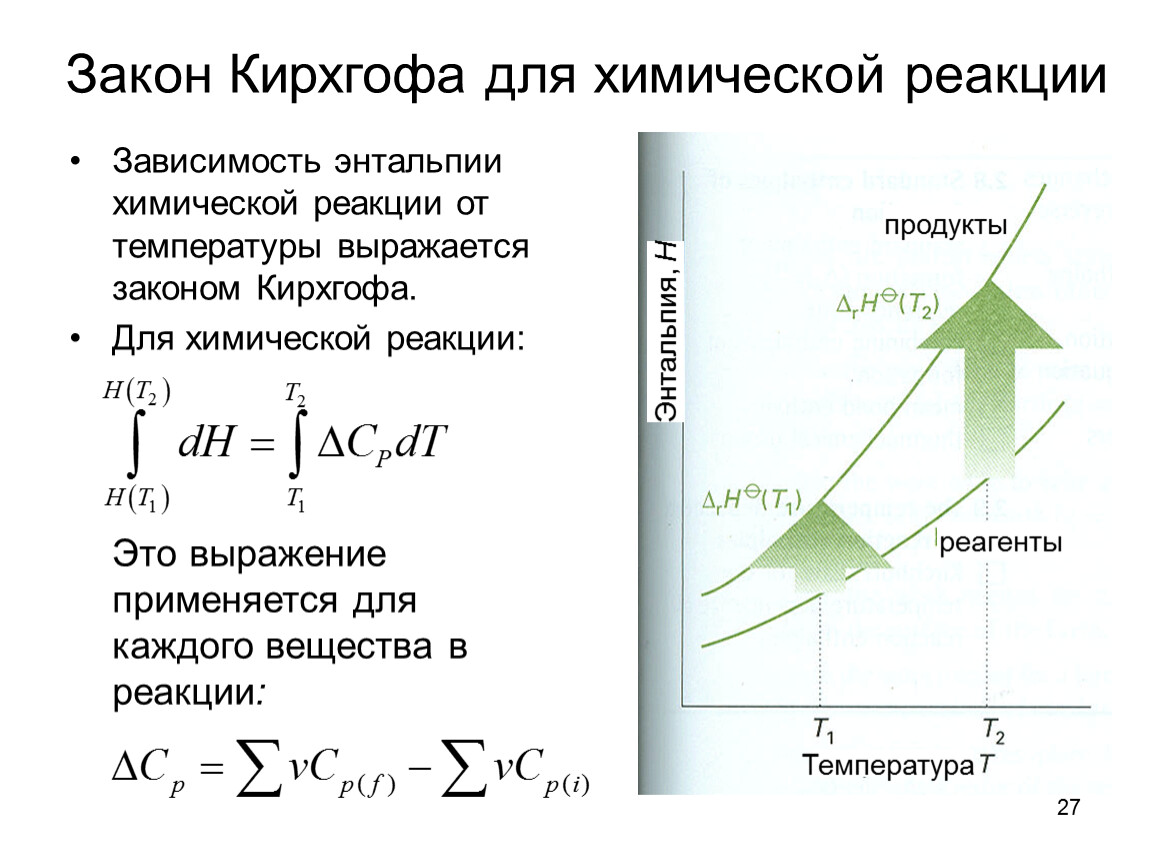
Принято в физике сплошных сред , термодинамике и статистической физике для той части полной энергии термодинамической системы , которая не зависит от выбора системы отсчета [1] и которая в рамках рассматриваемой задачи может изменяться [2]. То есть для равновесных процессов в системе отсчета, относительно которой центр масс рассматриваемого макроскопического объекта покоится, изменения полной и внутренней энергии всегда совпадают. Перечень составных частей полной энергии, входящих во внутреннюю энергию, непостоянен и зависит от решаемой задачи. Иначе говоря, внутренняя энергия — это не специфический вид энергии [3] , а совокупность тех изменяемых составных частей полной энергии системы, которые следует учитывать в конкретной ситуации. Внутренняя энергия как специфическое для термических систем понятие, а не просто как термин для обозначения изменяемой части полной энергии, нужна постольку, поскольку с её помощью в физику вводят новые величины: термические температура , энергия Гельмгольца , энтальпия и энтропия и химические химические потенциалы и массы составляющих систему веществ , энергия Гиббса [4]. Деление полной энергии системы на потенциальную , кинетическую , внутреннюю и т.